Genetypowanie KIR (z ang. killer cell immunoglobulin-like receptor) oraz locus HLA-C jest bardzo pomocne w diagnozowaniu przyczyn problemów z implantacją zarodka, występowania nawykowych poronień, tzn. takich, które występują co najmniej 3 razy pod rząd, oraz występowania poronień idiopatycznych, czyli poronień o niewyjaśnionej etiologii.
Geny KIR zlokalizowane są na chromosomie 19 (19q13.4). Do tej pory udało się wyróżnić 16 rodzajów tego typu genów. U ludzi może występować różna liczba genów KIR, charakterystyczny jest też tzw. polimorfizm alleliczny, czyli duże zróżnicowanie tych genów.
Znaczenie genów KIR
Geny KIR mają bardzo duże znaczenie, kodują bowiem obecność receptorów, które występują na powierzchni komórek NK. Receptory te mogą mieć działanie hamujące lub aktywujące. W zależności od obecności lub nieobecności kodujących je genów hamujących lub aktywujących, receptory występują w haplotypach A lub w haplotypach B. Do tej pory udało się wyróżnić dwie główne grupy haplotypów: AA i Bx. W grupie AA występuje więcej receptorów hamujących, natomiast grupa Bx odznacza się większą różnorodnością obecnych genów, ponieważ znajdują się w niej zarówno receptory hamujące, jak i receptory aktywujące.
Zgodnie z wynikami najnowszych badań, obecność u matki haplotypu hamującego AA oraz antygenu HLA-C2 na powierzchni trofoblastu (szczególnie jeśli jest on odziedziczony po ojcu), powiązane ze stanem przedrzucawkowym, problemami z prawidłowym zagnieżdżeniem się zarodka, możliwością wystąpienia ewentualnych poronień nawykowych oraz niewłaściwego odżywienia płodu.
Wykonanie genotypowanie KIR oraz genotypowanie locus HLA-C
Materiałem do badania genów KIR jest krew żylna pacjenta.
Krew jest pobierana w każdy wtorek w godzinach od 08:00 do 17:30.
Nie ma konieczności wcześniejszego umawiania wizyty.
Badanie AMH jest jednym z podstawowych rodzajów badań wykonywanych w diagnostyce niepłodności u kobiet. AMH to hormon antymullerowski, który jest należącą do rodziny transformujących czynników wzrostu homodimeryczną glikoproteiną. AMH pełni u kobiet bardzo ważną rolę w folikulogenezie jajnikowej. Stężenie AMH w surowicy okazuje się być relatywnie stabilne w trakcie cyklu miesiączkowego; do jego znaczniejszych zmian dochodzi u młodszych kobiet. Stężenie AMH wykazuje mniejsze wahania w trakcie cyklu czy pomiędzy cyklami niż podstawowe stężenie FSH. Stężenia AMH znacząco spada podczas stosowania antykoncepcji farmakologicznej dwuskładnikowej. Badanie AMH może być wykonywane zarówno w trakcie cyklu, jak i w przerwach pomiędzy cyklami.
Oznaczenie stężenia hormonu AMH jest wykonywane na w pełni automatycznym analizatorze cobas e411 firmy Roche, po wcześniejszym pobraniu krwi.
Najczęstszymi wskazaniami do badania AMH są ocena rezerwy jajnikowej oraz osiągnięcie przewidywanej odpowiedzi na kontrolowaną stymulację jajników. Oznaczenie AMH jest tez przydatne w diagnostyce PCOS oraz w przewidywaniu początku menopauzy.
Hormony FSH należą do rodziny gonadotropin. Obecność FSH stymuluje i wpływa na wzrost gonad, czyli jajników i jąder. U kobiet, hormony FSH działają na osi podwzgórze – przysadka – jajniki. Hormony FSH uwalniane są pulsacyjnie z komórek gonadotropowych przedniego płata przysadki mózgowej. Ich poziom reguluje stężenie hormonów sterydowych na drodze ujemnego sprzężenia zwrotnego z podwzgórzem. Rolą hormonów FSH u kobiet jest regulowanie cyklu menstruacyjnego. Wraz z hormonami LH, stymulują w jajnikach rozwój oraz dojrzewania pęcherzyków, dzięki czemu dochodzi w nich do biosyntezy estrogenów. Najwyższe stężenie hormonów FSH występuje w połowie cyklu miesiączkowego, wzrost ten jest nieco mniej wyraźny niż w przypadku hormonów LH, jednak znacznie wyraźniejszy niż w przypadku AMH. Wysokie stężenie FSH pojawia się w okresie menopauzy i jest związane z wygasaniem czynności jajników i niskim stężeniem estrogenów. U mężczyzn wysokie stężenie FSH może natomiast powodować rozwój spermatogonium.
Badanie polegające na oznaczeniu stężenia FSH w połączeniu ze stężeniem LH jest wykonywane przede wszystkim w diagnostyce chorób wrodzonych związanych z aberracją chromosomalną, diagnostyce zespołu PCO, do wyjaśniania przyczyn braku miesiączkowania i objawów przekwitania oraz w procedurach związanych z In Vitro.
Hormony LH, podobnie jak hormony FSH, należą do rodziny gonadotropin. Ich obecność wpływa na stymulowanie wzrostu gonad, czyli jajników i jąder. Ich rola i proces powstawania jest podobny, jak w przypadku hormonów FSH. Razem z nimi LH pełnią też taką sama rolę regulowania cyklu menstruacyjnego. Razem z nimi stymulują także rozwój i dojrzewanie pęcherzyków, co doprowadza do biosyntezy estrogenów.
Hormony LH osiągają najwyższe stężenie w połowie cyklu i prowadzą do jajeczkowania oraz powstawania ciałka żółtego, które wydziela progesteron. U mężczyzn w znajdujących się w jądrach komórkach Leydiga, hormony LH stymulują produkcję testosteronu.
Wysokie stężenie hormonów LH pojawia się w okresie menopauzy ze względu na wygasanie czynności jajników i niskie stężenie estrogenów. Oznaczanie stężenia LH w połączeniu z oznaczaniem stężenia FSH stosuje się w diagnostyce chorób wrodzonych związanych z aberracją chromosomalną, zespołu PCO oraz w ramach procedury In Vitro. Wskazaniem do badania może być także chęć wyjaśnienia braku miesiączki oraz pierwszych objawów przekwitania.
Estrogeny (przede wszystkim będący głównym elementem przeprowadzanego badania estradiol 17β) odpowiadają za rozwój drugorzędowych kobiecych cech płciowych. Estrogeny wspólnie z gestragenami kontrolują wszystkie procesy rozrodcze u kobiety. Wytwarzane są przede wszystkim w jajnikach (głównie w pęcherzykach i ciałku żółtym), niewielkie ilości estrogenów są także wytwarzane w korze nadnerczy. W trakcie ciąży powstają w łożysku, natomiast u mężczyzn produkcja estrogenów odbywa się w jądrach.
Stężenie estrogenów u kobiet jest zależne od fazy cyklu miesiączkowego. Ich wydzielanie podczas cyklu odbywa się bowiem dwufazowo. Bardzo duże zmiany w zależności od fazy cyklu sprawiają, że badanie stężenia estriadolu musi być wykonywane w ściśle określonych dniach cyklu, a wyniki badania odnosi się do zakresów stworzonych dla poszczególnych etapów.
Wskazaniami do oznaczania stężenia estriadolu są głównie: ocena zaburzeń na osi podwzgórze – przysadka – gonady, diagnostyka guzów jajników i guzów jąder, ginekomastia, a także prognozowanie jakości oocytu i ocena prawdopodobieństwa poczęcia w przypadku technik rozrodu wspomaganego.
Gestagen progesteron to rodzaj hormonu sterydowego, który jest wytwarzany przede wszystkim w komórkach ciałka żółtego, a w okresie ciąży w łożysku. Wartość stężenia progesteronu jest więc zależna od fazy rozwoju ciałka żółtego. W fazie pęcherzykowej progesteron jest prawie nieoznaczalny, natomiast w dzień przed jajeczkowaniem jest go już bardzo dużo. Jego wzmożona synteza następuje w fazie lutealnej.
Progesteron pełni bardzo ważną role. W fazie wydzielniczej jest bowiem odpowiedzialny za przekształcanie śluzówki macicy w tkankę, która jest bogata w gruczoły, a dzięki temu jest przygotowana do zagnieżdżenia zapłodnionego jajeczka. W trakcie ciąży z kolei, progesteron hamuje skurcze miometrium. Progesteron pełni również ważną funkcję w gruczołach mlekowych. Wzmaga w nich proliferację i możliwości wydzielnicze pęcherzyków.
Badania oznaczania progesteronu wykonuje się w celu dokonania oceny indukcji owulacji. Badanie jest także bardzo ważne do monitorowania terapii zastępczej progesteronem oraz do wykrywania i oceny ryzyka poronienia we wczesnym okresie ciąży. Jeśli nie dochodzi do zapłodnienia, stężenie progesteronu bardzo szybko opada do swojej wyjściowej fazy folikularnej. Jest to więc niezawodna metoda, która pozwala na stwierdzenie owulacji.
Testosteron ma bardzo duże znaczenie w płodności mężczyzn. Jest u nich niemal w całości wytwarzany w komórkach Leydiga w jądrach. Jego wydzielanie jest regulowane przez hormony LH i może podlegać hamowaniu zwrotnemu ze strony przysadki i podwzgórza. Rolą testosteronu u mężczyzn jest wspomaganie rozwoju drugorzędowych cech płciowych i podtrzymywanie czynności prostaty oraz pęcherzyków nasiennych.
Wskazaniami do wykonania badania pomiaru testosteronu całkowitego u mężczyzn mogą być androgenizacja mężczyzn, nieprawidłowa lub niewystarczająca czynność jąder, zaburzenia płodności, objawy wirylizacji, a także nowotwór jąder lub nowotwór nadnerczy.
Testosteron jest obecny także u kobiet. Jego niewielkie ilości są wytwarzane w jajnikach. W stężeniu fizjologicznym ich obecność nie powoduje żadnych szczególnych efektów. Wytwarzanie zbyt dużej ilości testosteronu u kobiet może jednak prowadzić do maskulinizacji, do powstawania zespołu policystycznych jajników, zaburzeń płodności, przerostu nadnerczy, a nawet do nowotworów jajników.
Prolaktyna w surowicy krwi występuje w trzech różnych formach. Przeważającą biologicznie i immunologicznie jest aktywna forma monomeryczna (tzw. mała), która stanowi niemal 80 proc. Prolaktyna jest wydzielana partiami w przednim płacie przysadki. Głównym działaniem hormonu jest wspomaganie rozwoju i różnicowanie gruczołu mlekowego. Wysokie stężenie prolaktyny powoduje hamowanie sterydogenezy jajników oraz produkcję i wydzielanie ganadotropin przysadkowych. W trakcie ciąży stężenie prolaktyny wzrasta na skutek działania estrogenu i progesteronu. Dzięki stymulacyjnemu działaniu prolaktyny na gruczoł mlekowy, po porodzie może występować laktacja.
Oznaczanie stężenia prolaktyny jest u kobiet wykonywane w celu rozpoznania cykli bez jajeczkowania, w diagnozowaniu braku miesiączki spowodowanej nadmiarem prolaktyny i mlekotoku, a także w diagnostyce ginekomastii oraz przy podejrzeniu nowotworu piersi lub guza przysadki. U mężczyzn badanie stężenia prolaktyny wykonuje się w diagnostyce azoospermii.
Zarówno u kobiet, jak i u mężczyzn może dochodzić do powstawania hiperprolaktynemii. Może być to główną przyczyną zburzeń płodności (u mężczyzn może np. hamować sekrecję testosteronu). Istnieją dwie formy hiperprolaktynemii: organiczna i czynnościowa. Do ich diagnostyki niezbędne jest wykonanie niezbędnych badań, zgodnie z zaleceniami lekarza.
W diagnostyce przyczyn niepłodności bardzo ważne jest także oznaczenia hormonów tarczycy. Jednym z najważniejszych jest tyreotropina TSH, czyli hormon odpowiedzialny za stymulowanie pracy tarczycy. Do jego powstawania dochodzi w komórkach swoistych przedniego płata przysadki mózgowej. Jego wydzielanie z przysadki odbywa się w sekwencjach dobowych. Czym jest TSH? Hormon ten jest centralnym mechanizmem, który jest odpowiedzialny za biologiczne regulowanie działania hormonów tarczycy na wszystkich etapach ich wytwarzania i wydzielania. TSH ma także działanie proliferacyjne.
Oznaczanie stężenia TSH jest wstępnym badaniem przesiewowym w rozpoznawaniu różnego typu chorób tarczycy. Nawet niewielkie zmiany w stężeniu wolnych hormonów tarczycy mogą powodować powstawanie odwrotnych zmian stężenia hormonów TSH. Oznaczanie stężenia TSH jest bardzo czułym i swoistym parametrem pozwalającym ocenić czynność tarczycy. Umożliwia m.in. wczesne rozpoznanie lub wykluczenie zaburzeń osi pomiędzy podwzgórzem, przysadką i tarczycą.
Badanie Anty-Tpo to Ilościowe oznaczanie In vitro stężenia przeciwciał przeciwko tyreoperoksydazie. Badanie to jest wspomagające w rozpoznaniu autoimmunologicznych chorób tarczycy, tzn. takich w których organizm działa przeciwko sobie. TPO może być bowiem potencjalnym autoantygenem. Podwyższone stężenie w surowicy przeciwciał przeciwko TPO może występować w co najmniej kilku formach autoimmunologicznego zapalenia tarczycy, m.in. w chorobie Hashimoto, czy Graves-Basedowa.
Czułość badania Anty-Tpo można jeszcze zwiększyć poprzez jednoczesne oznaczanie przeciwciał anty-Tg lub przeciwciał przeciwko receptorowi TSH-TRAb. Trzeba jednak pamiętać o tym, że ujemny wynik testu wcale nie wyklucza możliwości występowania choroby autoimmunologicznej. Miano przeciwciał nie wykazuje bowiem zależności z kliniczną aktywacją choroby. Stwierdzenie obecności oraz podwyższonego stężenia tego przeciwciała dowodzi tylko reakcji układu odpornościowego na tkankę tarczycową. Proces ten jednak może wywołać chorobę lub też nie.
Rola oznaczeń przeciwciał anty-TPO, czyli oznaczeń przeciwtarczycowych oraz diagnostyki choroby Hashimoto jest bardzo duża, ponieważ są to pierwsze i jednocześnie najbardziej dostępne, najbardziej znane i jedne z najtańszych badań w kierunku zaburzeń układu immunologicznego. Trzeba bowiem pamiętać, że często to właśnie choroba Hashimoto lub tylko podwyższony poziom przeciwciał anty-TPO jest pierwszą wskazówką, że przyczyna problemów z zajściem w ciążę wiąże się z problemami układu odpornościowego.
Witamina D jest produkowana pod wpływem promieni słonecznych w skórze. Jest rozpuszczalnym w tłuszczach prekursorem hormonów sterydowych. Biologicznie witamina ta jest nieaktywna, żeby zostać aktywowana musi być poddana dwóm kolejnym hydroksylacjom, najpierw w wątrobie, a potem w nerkach. Rola witaminy D jest bardzo duża, wykazano jej wpływ na ekspresję ponad 200 różnych genów. Niedobory witaminy D są łączone z powstawaniem cukrzycy, różnych postaci chorób nowotworowych, chorób autoimmunologicznych, chorób układu krążenia i chorób, które przebiegają wraz z zaburzeniami odporności.
Witamina D ma także, wspólnie z hormonami sterydowymi, czyli klasycznymi regulatorami układu rozrodczego, duży wpływ na funkcje rozrodcze kobiet i mężczyzn. Zmiany w stężeniu witaminy D w surowicy krwi mają wpływ na rozrodczość zdrowych kobiet, jednak szczególne znaczenia mają w przypadku pacjentek, które są poddawane procedurom wspomaganego rozrodu, pacjentek z PCOS oraz pacjentek z endometriozą. Stężenie wit. D wykazuje oczywiście zależność sezonową związaną z ilością nasłonecznienia. Wyższe jej stężenia są notowane latem i na jesieni, natomiast niższe zimą i wiosną.
Biocenozę pochwy inaczej nazywa się także: biologią pochwy, oceną stopnia czystości pochwy, badaniem flory pochwy lub rozmazem z pochwy. Celem przeprowadzenia badania jest dokładne sklasyfikowanie zasiedlających nabłonek pochwy populacji drobnoustrojów, czyli tzw. biofilmu. Poznanie dokładnego składu gatunkowego, dynamiki oraz struktury biofilmu ma bardzo duże znaczenie dla zdrowia i czynności narządu rodnego.
Trzeba bowiem wiedzieć, że środowisko pochwy stanowi u kobiety samodzielną biocenozę, której najistotniejszym składnikiem są pałeczki kwasu mlekowego, czyli pałeczki Doderleina Lactobacillus acidophilus, L. fermentum itp. Są one Gramm dodatnie i mogą występować w różnych postaciach (małych, średnich i olbrzymich). Bakterie te pełnią ważną funkcję, chroniąc nabłonek pochwy przed innymi drobnoustrojami, przede wszystkim przed tymi, które są chorobotwórcze. Pałeczki kwasu mlekowego mają także zdolność produkcji nadtlenku wodoru, który także stanowi barierę ochronną.
Z racji pełnionych roli, ilość i jakość pałeczek kwasu mlekowego świadczy o stanie fizjologicznym pochwy. Wykonanie badania biocenozy pochwy pozwala sprawdzić czy wszystko jest w należytym porządku i czy utrzymana jest równowaga środowiska pochwy, czyli m.in. zachowana jest właściwa kwasowość czy właściwa ilość nadtlenku wodoru. Pałeczki kwasu mlekowego, poprzez swoją obecność, stymulują również układ odpornościowy.
Kariotyp określa kompletny zestaw chromosomów, czyli materiału genetycznego wewnątrz komórki. Kariotyp to zarówno chromosomy autosomalne (22 pary chromosomów), jak i chromosomy płciowe (1 para XX lub XY). Określanie kariotypu to rodzaj badania cytogenetycznego, czyli z zakresu genetyki zajmującej się badaniem chromosomów. Dziedzina ta koncentruje się nie tylko na badaniu kształtu oraz liczby chromosomów, ale także na ich dziedziczeniu.
Badanie chromosomów przeprowadza się w co najmniej kilku przypadkach, przede wszystkim w przypadku podejrzenia występowania choroby genetycznej, która mogłaby być spowodowana zaburzeniami w liczbie lub strukturze chromosomów. Określenie kariotypu wykonuje się także w przypadkach nawykowych poronień, jest to także ważne badanie prenatalne u kobiet po 37. roku życia, a także w przypadku wystąpienia niektórych chorób nowotworowych (wykrycie nieprawidłowego kariotypu może ułatwić identyfikację i leczenie guza).
Obecność mutacji genu CFTR jest odpowiedzialna za powstawanie mukowiscydozy. Częstość występowania tej choroby szacuje się na 1/2500 żywych urodzeń. Jest to bardzo ciężkie schorzenie wieloukładowe z licznymi objawami ze strony układu pokarmowego, układu oddechowego oraz układu moczowo-płciowego. Organizm osoby chorej na mukowiscydozę produkuje nadmiernie lepki śluz, który powoduje powstawanie zaburzeń we wszystkich narządach śluzowych.
Mutacje w genie CFTR mogą mieć także inne konsekwencje. U mężczyzn mogą być przyczyną niektórych form niepłodności, np. obustronnej niedrożności lub braku przewodów nasiennych oraz azoospermii obstrukcyjnej. Obok mukowiscydozy istnieje także cała grupa innych chorób, które mogą być spowodowane mutacjami w/w genie.
Wykonanie badania genetycznego mutacji CFTR jest obecnie standardem w procedurze wspomaganego rozrodu. Celem wykonywanego badania jest próba ustalenia przyczyn niepłodności męskiej oraz określenie prawdopodobieństwa urodzenia się dziecka chorego na mukowiscydozę. Według prowadzonych badań, prawie 95 proc. mężczyzn z CF może być niepłodna z powodu azoospermii spowodowanej włóknieniem, procesem zanikowym (atrofią), lub całkowitym już brakiem najądrza, nasieniowodów, czy pęcherzyków nasiennych. Co więcej może to być jedyny objaw nietypowej postaci CF.
U kobiet z powodu CF zapłodnienie może być utrudnione na skutek zbyt gęstego śluzu w szyjce macicy.
Trombofilia, czyli nadkrzepliwość to choroba w efekcie której następuje zbyt duża krzepliwość krwi i zachodzi skłonność do tworzenia się skrzepów (przede wszystkim skrzepów żylnych w kończynach dolnych). Trombofilia jest szczególnie groźna u kobiet w ciąży, ponieważ może stać się przyczyną poronienia. Choroba ta może występować w postaci nabytej lub w postaci wrodzonej. Trombofilia wrodzona ma podłoże genetyczne. Najczęściej jest konsekwencją mutacji genu protrombiny lub czynnika V układu krzepnięcia (tzw. V Leiden). Wykonanie badania DNA zleca się przede wszystkim kobietom które mają problemy z zajściem w ciążę, przyjmującym doustną antykoncepcję hormonalną oraz takim, które stosują hormonalną terapię zastępczą. Dokładny opis możliwych mutacji genów, które mogą mieć wpływ na obecność choroby, znajdą Państwo w zakładce na temat badań genetycznych w kierunku trombofilii wrodzonej.
Zespół genów AZF (ang. azoospermia factor) jest ulokowany na męskim chromosomie Y, a konkretnie na jego długim ramieniu, które ma szczególne znaczenie dla męskiej płodności. Nawet drobne mutacje w obrębie rejonu AZF prowadzą bowiem do zaburzeń w produkcji plemników (spermatogenezie), która objawia się jako azoospermia (stan w którym jest brak plemników w nasieniu) lub oligozoospermia. Oba te stany są częstą przyczyną niepłodności u mężczyzn. Ocenia się nawet, że mutacje te są drugą co do częstości (zaraz po zespole Klinefeltera) genetyczną przyczyną męskiej niepłodności. Badanie genetyczne AZF wykonywane jest w celu wykrycia ewentualnych mutacji na chromosomie Y.
Makroprolaktyna jest agregatem nieco bardziej złożonym od omawianej wcześniej prolaktyny, w której w aż 80 proc. przeważa, aktywna biologicznie i immunologicznie, mała forma monometryczna PRL. Makroprolaktyna jest agregatem o wyższym ciężarze cząsteczkowym, który składa się z PRL we wszystkich formach oraz z przeciwciał klasy IgG. W tworzeniu obecnych w makroprolaktynie wysokocząsteczkowych agregatów PRL biorą także udział rozpuszczalne, krótkie formy receptora, które dla PRL są często utożsamiane z białkiem wiążącym prolaktynę (czyli PBP – prolactin binding protein). U osób z hiperprolaktynemią występowanie makroprolaktyny nie jest zjawiskiem rzadkim. Określenie procentowego udziału makroplaktyny może być bardzo przydatne zarówno w diagnozowaniu, jak i w wyborze najbardziej optymalnego sposobu leczenia.
HCG to ludzka gonadotropina kosmówkowa. Fizjologicznie HCG jest wytwarzana przez łożysko u kobiet w ciąży. Z kolei u kobiet niebędących w ciąży, może być wytwarzana przez guzy trofoblastów, guzy drobnokomórkowe z elementami trofoblastycznymi oraz przez niektóre rodzaje guzów nietrofroblastycznych. Biologiczną rolą gonadotropin HCG jest podtrzymywanie ciałka żółtego podczas trwania ciąży. HCG wpływa także na wytwarzanie sterydów. Podwyższone wartości stężenia HCG mogą wskazywać na nowotwór kosmówki, zaśniad groniasty lub na ciążę mnogą. Z kolei obniżone wartości HCG mogą świadczyć o zwiększonym niebezpieczeństwie poronienia, poronieniu chybionym, ciąży pozamacicznej, gestozie lub o obumarciu płodu. Oznaczanie HCG+β jest również częścią oceny ryzyka trisomii 21.
Testy βHCG służą przede wszystkim jako test ciążowy do wczesnego wykrywania i monitorowania ciąży. Po implantacji zapłodnionej komórki jajowej, czyli pomiędzy 6 a 8 dniem owulacji, już zaledwie 48 godzin później we krwi pojawia się mierzalne stężenie HCG. Oprócz tego test βHCG jest także stosowany, w połączeniu z innymi testami, do oceny ryzyka trisomii 21. Jest także użyteczny w monitorowaniu pacjentów z chorobami trofoblastycznymi oraz może służyć do wykrywania i monitorowania komórek nowotworowych, które produkują HCG w jajnikach, jądrach lub w łożysku. Test polega na pobraniu próbki krwi.
Tyroksyna FT4 to jeden z hormonów tarczycy, który może wpływać na metabolizm ustroju. Większość hormonu FT4 w organizmie człowieka jest związana z białkami transportującymi, czyli z TBG, prealbuminą czy albuminą. Wolna tyroksyna FT4 jest fizjologicznie aktywną częścią tyroksyny, tzn. że jej stężenie nie zależy od zmian białek wiążących, ani od ich właściwości wiążących. Oznaczanie stężenia FT4 wykonuje się przede wszystkim w sytuacjach podejrzenia zaburzeń czynności tarczycy. Badanie wykonywane jest wówczas łącznie z oznaczaniem TSH. Oznaczanie FT4 jest także wykonywane w monitorowaniu terapii tyreosupresyjnej. Wzrost stężenia FT4 jest charakterystyczny dla nadczynności tarczycy, natomiast jego spadek dla jej niedoczynności.
AFP, czyli Alafa1 fetoproteina, jest podobną do albuminy glikoproteiną. AFP może być wytwarzana w pęcherzyku żółciowym, w niezróżnicowanych komórkach wątroby, a także w przewodzie pokarmowym płodu. Podwyższone stężenie AFP we krwi występuje aż u 70-95 proc. pacjentów, u których zdiagnozowano nowotwór pierwotny komórek wątroby. Wartości stężenia AFP wzrastają wraz ze stopniem zaawansowania nowotworów drobnokomórkowych, które nie są nasieniakami.
AFP, obok ludzkiej gonadropiny kosmówkowej, są bardzo ważnymi parametrami, które pozwalają ocenić szanse przeżycia pacjentów z niebędącymi nasieniakami, zaawansowanymi guzami drobnokomórkowymi. Znacznie podwyższone stężenie AFP może wskazywać na pierwotny nowotwór komórek wątroby, natomiast u kobiet w ciąży, w surowicy krwi lub w płynie owodniowym, może wskazywać na rozszczep kręgosłupa, bezmózgowie, niedrożność przełyku lub ciążę mnogą. Oprócz tego oznaczanie AFP jest także częścią oceny ryzyka trisomii 21. Badanie polega na pobraniu próbki krwi.
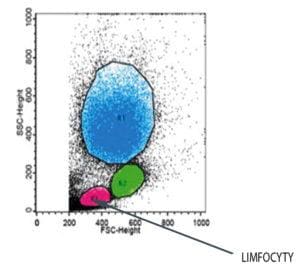
Celem wykonania oceny subpopulacji limfocytów T, B oraz komórek NK jest ocena liczby i odsetka limfocytów T (Th, Ts/c), B oraz komórek NK, w celu określenia stanu immunologicznego organizmu. Badanie to jest wykonywane metodą wielokolorowej cytometrii przepływowej, przy użyciu certyfikowanych odczynników, zawierających przeciwciała monoklonalne skierowane przeciwko badanym antygenom.
| PARAMETR | NAZWA KOMÓREK | SZCZEGÓŁOWA CHARAKTERYSTYKA KOMÓREK |
| CD3+ | Limfocyty T | Limfocyty T– komórki układu odpornościowego odpowiedzialne za komórkową odpowiedź immunologiczną. Istnieje kilka różnych typów limfocytów T i maja one różne funkcje. Komórki te wywierają swoje działanie albo przez uwalnianie rozpuszczalnych białek, zwanych cytokinami, które są sygnałami dla innych komórek, albo przez bezpośrednie interakcje komórka – komórka |
| CD3+4+ | Limfocyty Th | Limfocyty T pomocnicze(Th) – wytwarzają cytokiny dzięki którym współdziałają z limfocytami B i pomagają im dzielić się, różnicować i tworzyć przeciwciała. Współdziałają także z jednojądrzastymi fagocytami i pomagają im zniszczyć patogeny wewnątrzkomórkowe. |
| CD3+8+ | Limfocyty Ts/c | Limfocyty T supresorowe/cytotoksyczne (Ts/c)-odpowiedzialne są za niszczenie komórek gospodarza, które zostały zakażone przez wirusy lub inne wewnątrzkomórkowe patogeny – działanie takie zwane jest cytotoksycznością. |
| CD3-19+ | Limfocyty B | Limfocyty B – każda komórka B ma genetycznie zaprogramowaną informacje o strukturze receptora powierzchniowego dla jakiegoś szczególnego antygenu. Po rozpoznaniu swoistego antygenu limfocyty B mnożą się i różnicują do komórek plazmatycznych, które produkują duże ilości cząsteczek wydzielanego receptora w formie rozpuszczalnej. Znane są one jako przeciwciała. Cząsteczki przeciwciał są wielkimi glikoproteinami znajdującymi się w krwi i płynach tkankowych; ponieważ są całkowicie identyczne z oryginalnymi cząsteczkami receptorowymi, wiążą antygen, który zapoczątkował pobudzenie limfocytów B. |
| CD3-16+i/lub CD56+ | Komórki NK | Komórki NK (Natural Killer) – mają również zdolność rozpoznawania zmian rozpoznawania zmian powierzchniowych, jakie zachodzą na różnych komórkach nowotworowych i komórkach zakażonych przez wirusy. Komórki NK niszczą te komórki docelowe, ale odmiennie niż komórki Ts/c. Stosują raczej nieswoiste systemy rozpoznawania. Działanie to nazywane jest niekiedy aktywnością komórek naturalnych zabójców. Mogą również rozpoznawać i niszczyć niektóre komórki docelowe (lub patogeny), które zostały opłaszczone swoistymi przeciwciałami. |
| CD3-16+i/lub CD56+ | Komórki NK | Limfocyty NKT (Natural Killer T-cells) – posiadają markery powierzchniowe charakterystyczne dla limfocytów T i komórek NK. Mają właściwości zarówno cytotoksyczne jak i immunoregulacyjne, |
| Th/Ts | Proporcja limfocytów Th/Ts (ratio) | |
| SUMA limfocytów T, B i kom. NK | Kontrola badania | Powinna mieścić się w zakresie 95-105. Nieprawidłowości fenotypowe skutkujące obniżeniem lub podwyższeniem sumy spotykamy w niedoborach immunologicznych a także w nowotworowych rozrostach wywodzących się z komórek limfoidalnych (gł. chłoniaki) |
| CD5+19+ | Limfocyty B1 | Limfocyty B1 – są odpowiedzialne za odporność wrodzoną, produkują przeciwciała m. in. przeciwko hormonom, receptorom i neurotransmiterom w mechanizmie niezależnym od limfocytów T. Ich ciągłe pobudzenie oraz możliwość wiązania fizjologicznych ligandów jest prawdopodobnie przyczyną ich częstego występowania w formie autoagresywnych komórek w chorobach autoimmunizacyjnych. |
Wskazania do wykonania badania immunofenotypu, czyli oceny subpopulacji limfocytów T (Th, Ts/c), B i komórek NK mogą być różne. Przede wszystkim są to niepowodzenia z zajściem w ciążę, poronienia, niepowodzenia przy wspomaganym rozrodzie, pierwotne i wtórne niedobory odporności, zaburzenia immunologiczne oraz leuko/limfocytoza lub leuko/limfopenia przy braku stwierdzonego czynnika sprawczego.
Przygotowania do badania immunofenotypu
Pacjentka, która zgłasza się na badanie immunofenotypu powinna być na czczo. Badanie wykonywane jest w dniu pobrania, z krwi żylnej pacjentki. W naszym laboratorium diagnostycznym w szczególny sposób dbamy o prawidłowe pobranie krwi do tego badania. Pacjentki są zawsze umawiane na pobranie materiału na konkretne godziny poranne. Równocześnie wykonywane jest badanie morfologii krwi dla ilościowego określenia badanych typów limfocytów.
Znaczenie oceny subpopulacji limfocytów T, B i komórek NK w nawykowych poronieniach
W przypadku nawykowych poronień, tzn. takich które występują przynajmniej trzy razy pod rząd, bardzo często obserwuje się zaburzenia w liczebności oraz w proporcjach pomiędzy poszczególnymi subpopulacjami limfocytów.
W naszym Centrum Medycznym w diagnostyce patogenów przenoszonych drogą płciową wykorzystujemy metodę PCR (ang. Polimerase Chain Reactions), czyli reakcję łańcuchowej polimerazy. Badamy obecność m.in. następujących patogenów:
• Chlamydia trachomatis,
• Mycoplasma hominis,
• Ureaplasma spp.
Metoda PCR umożliwia nam oznaczanie tych patogenów poprzez badanie obecności w materiale ich DNA, a nie poziomu przeciwciał. Dzięki temu możliwe jest uzyskanie jednoznacznego wyniku oraz wykrycie infekcji w postaci zakażenia urogenitalnego we wczesnym jej etapie. Wysoka czułość badania metodą PCR umożliwia wykrycie nawet pojedynczych komórek bakterii.
Ekstrakcja kwasów nukleinowych, czyli Izolacja materiału genetycznego z pobranej próbki jest w pełni automatyczna dzięki użyciu urządzenia SaMag firmy Sacace Biotechnologies z zastosowaniem kuleczek separujących. Takie działanie zapewnia wysoką jakość badań, bezpieczeństwo pobranych próbek oraz najwyższą wiarygodność wyników.



